Смола из Колофона
Семь городов Древней Греции оспаривали честь быть родиной великого Гомера. Аргос, Афины, Колофои, Родос, Саламин, Смирна и Хиос. Лишь один из них интересует нас сейчас, в связи с темой нашего рассказа, — малоазийский город Колофон. Много веков назад из него вывозили твердый продукт, который получали из живицы, жидкости, вытекающей из надрезов на сосновом стволе. Искаженное название этого города дало имя желто-коричневой смоле, которую ныне получают в самых разных краях света, и что ни год то больше, — всем известной канифоли.
О СМОЛАХ ВООБЩЕ И КАНИФОЛИ В ЧАСТНОСТИ
Прежде всего заметим, что термин «смола» отнюдь не химический. С давних времен так характеризовали вещества с высокой липкостью (вспомните поговорку — «прилип как смола»). В разряд смол попали самые разные вещества — от обычной канифоли до какого-нибудь экзотического сандарака.
Попытаемся ввести в древнее понятие «смола» химическое содержание.
Смолы — не индивидуальные вещества, а смеси. Правда, входящие в их состав соединения обычно близки по химической природе, например, это могут быть гомологи или даже изомеры. Молекулярный вес таких веществ не очень велик — от 100 до 1000, и связаны они между собой не химически, а только молекулярными силами. Это и отличает их от многочисленных полимеров, как натуральных (каучук, гуттаперча), так и синтетических (полиэтилен, полипропилен, полистирол и т. п. ). Как и названные полимеры, природные смолы термопластичны, то есть они плавятся при нагревании, а охлаждаясь, вновь затвердевают Они способны растворяться в расплавах полимеров, в восках и жирах; при этом молекулярные связи заметно ослабляются, и в растворе появляются свободные молекулы. Именно это и предопределило назначение .многих смол: свободные молекулы, выходя на поверхность с солидным запасом свободной энергии, создают липкость, то самое свойство смол, которое более всего интересует технологов, особенно если они работают с клеями.
Теперь перейдем от смол вообще к конкретной смоле — канифоли. Она образует свободные молекулы не только в растворах и расплавах, но и при механическом воздействии. Когда смычок натирают канифолью, а затем проводят им по струнам, свободные молекулы взаимодействуют со струной, создавая известное сцепление, струна начинает вибрировать — и льется музыка. Свободные молекулы канифоли при трении придают временную, мгновенную липкость подошвам, и боксер не скользит на ринге, жокей — на крупе лошади.
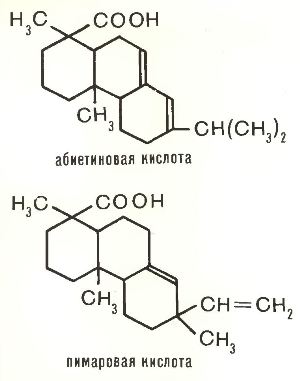 Какие же молекулы сообщают канифоли такие свойства?
В первую очередь — абиетиновой и пимаровой кислот. Они похожи, и различие между ними заключается лишь в
боковых углеводородных группах. Обе эта кислоты — типичные представители целого
ряда соединений, которые отличаются друг от друга расположением боковых групп
и количеством двойных связей, поэтому о них нередко говорят во множественном
числе — абиетиновые и пимаровые кислоты.
Какие же молекулы сообщают канифоли такие свойства?
В первую очередь — абиетиновой и пимаровой кислот. Они похожи, и различие между ними заключается лишь в
боковых углеводородных группах. Обе эта кислоты — типичные представители целого
ряда соединений, которые отличаются друг от друга расположением боковых групп
и количеством двойных связей, поэтому о них нередко говорят во множественном
числе — абиетиновые и пимаровые кислоты.
Двойные связи имеют особое значение: благодаря им можно без большого труда менять структуру (а значит, и свойства) канифольных кислот. Например, их можно гидрировать, полимеризовать и, что наиболее важно, диспропорционировать. Поясним этот не всем понятный термин. В присутствии иодного катализатора нагретая канифоль существенно видоизменяется. Ее кислоты лишаются сопряженных двойных связей, и стойкость канифоли к окислению значительно увеличивается Это и есть диспропорционирование. Оно позволяет получить также жидкую канифоль, которую удобно транспортировать и смешивать.
Молекулярный вес компонентов канифоли невелик, в среднем, около 200. И хотя в молекулах кислот есть кислород, канифоль относят все же к углеводородным смолам, ибо скелет ее построен из молекул изопрена — того самого изопрена, который служит основой натурального каучука, копала и янтаря.
Разумеется, не только из кислот состоит канифоль. В ней есть немного углеводородов и других соединений, но все это не более чем примеси.
ОТ ДРЕВНОСТИ ДО НАШИХ ДНЕЙ
Начиналась канифоль с живицы, которую используют никак не менее трех тысяч лет. О живице журнал в свое время подробно писал (1971, № 4) и нет надобности долго говорить о ней здесь, заметим только, что еще Геродот упоминал скипидар, полученный из живицы, которую нагревали в котлах, покрытых бараньими шкурами. Жидкий продукт такой разгонки и есть скипидар, твердый же остаток — канифоль.
Но еще живицей называют осмол, который содержится в старых сосновых пнях Это ценное сырье, и чтобы извлечь его, пни расщепляют (сейчас — взрывчаткой). Пень разлетается в щепки, их собирают и живицу извлекают растворителями; ее называют поэтому экстракционной, и так же называют канифоль из пней.
Два эти способа были единственными вплоть до начала нашего века. Между тем хвойных лесов становилось все меньше а потребность в канифоли (по причинам, о которых будет рассказано ниже) непрерывно росла. Противоречие казалось неразрешимым. Впрочем, семьдесят лет назад не слишком над этим задумывались.
Как бы то ни было, в 1905 г. шведские специалисты по бумаге придумали способ, позволивший получать канифоль без рубки лесов специально для этой цели. Сосновая древесина расходуется в огромных количествах для производства бумаги, от этого никуда не деться — в ближайшем будущем, по крайней мере. Но бумажников интересует не древесина вообще, а только часть ее — волокна целлюлозы. Все остальное, в том числе и компоненты канифоли для целлюлозно-бумажной промышленности — балласт. Его надо удалить, и для этого древесину измельчают и обрабатывают раствором щелочи в которой целлюлоза не растворяется в отличие от лигнина, канифоли и жирных кислот.
Щелочной раствор канифоли и других веществ называют щелоком натронной варки. Многие десятилетия этот щелок был обременительным отходом бумажного производства, он отравлял жизнь не только технологам, но и — в самом прямом смысле слова — растениям и животным в окрестных водоемах.
Так вот, в 1905 г было установлено, что если подкислить упаренный под вакуумом щелок, то из него можно выделить смесь жирных кислот и канифоли. Сосна по-шведски «талл» (tall), а так как полученная смесь на ощупь масляниста, ее назвали сырым талловым маслом. Это своего рода живица, содержащая около 40% канифоли. Впрочем, техника фракционной разгонки не достигла в то время высокого уровня, и выделять отдельные составляющие из таллового масла в промышленном масштабе было делом нереальным. В лучшем случае это ценнейшее сырье использовали как топливо.
Лишь в 1950 г. был создан непрерывный способ разгонки таллового масла под высоким вакуумом (в так называемых молекулярных кубах). И с этого времени талловое масло стало важным сырьем для получения канифоли: из одной тонны масла извлекают более 360 кг смолы.
ЗАЧЕМ НУЖНА КАНИФОЛЬ
Разумеется, не только затем, чтобы натирать смычки и подошвы, — тогда проблемы не было бы вовсе, хватило бы на все про все старых пней.
Есть у канифоли традиционные области применения. Скажем, производство некоторых лаков, сургуча, пластырей. Прежде ее использовали в огромных количествах мыловары — канифоль отчасти заменяла жиры. Есть и забытые рецепты, скажем, колесной мази.
Мало помалу канифоль завоевывала новые позиции. Многие годы в масляные лаки н краски с повышенной твердостью и стойкостью к износу добавляли экзотические копалы. Россия импортировала немало копалов, главным образом для каретных лаков, к которым предъявлялись особо высокие требования. Автомобили сменили кареты, но и для них нужен был прочный лак. Лишь в 1930 г. был получен искусственный копал. Как читатель догадывается, без канифоли дело не обошлось — это был продукт ее взаимодействия с фенолальдегидной смолой.
Когда широко пошли в ход электрические лампы, возникла серьезная проблема: чем крепить стеклянные баллоны к металлическим цоколям? Существовало немало мастик, а цоколи тем не менее отваливались. Лишь введение в мастику канифоли позволило решить вопрос; ее применяют на электроламповых заводах с тридцатых годов и до наших дней.
Многие знают, что канифоль — отличный флюс для пайки и лужения металлов. С этой целью ее используют не только радиолюбители, но и заводские технологи. Менее известно (но не менее важно) применение канифоли в полиграфии без нее не обходится почти ни одна краска для глубокой печати и для плоской (которой, кстати, печатается «Химия и жизнь»; так что в строчках, которые вы читаете, тоже есть канифоль). Назначение канифоли логически вытекает из ее свойств: она закрепляет оттиснутые буквы и рисунки на бумаге.
Но, пожалуй, самый крупный потребитель смолы — бумажная промышленность. Любую бумагу (кроме, естественно, фильтровальной) приходится проклеивать, чтобы она стала гладкой и не впитывала воду. Канифоль — самый удобный для этой цели материал, ее соль (канифольное мыло) взаимодействует в бумажных волокнах с сульфатом алюминия, вторым компонентом проклейки, и образуется устойчивый и нерастворимый в воде комплекс.
НОВАЯ ИСТОРИЯ КАНИФОЛИ
Она началась в сороковых годах нашего века. Для товаров, которых становилось все больше, требовалась упаковка. Появились принципиально новые товары (скажем, препараты бытовой химии), которым нужна надежная и красивая упаковка; широкое распространение получили пищевые концентраты. Проблема тары и упаковки стала столь важной, что появилось множество исследовательских учреждений, которые ею занимаются, чуть не каждый год собираются конгрессы и симпозиумы.
Как сделать быстро (и не слишком расширяя заводские площади) много коробок, ящиков, пакетов, туб? Узкое место — сборка. Это справедливо и для многих других производств, например, швейного.
Казалось бы, сварка может оказаться подходящим методом, однако далеко не все поддается сварке (например, древесина и картон). Поэтому понадобились клеи, которые способны схватываться буквально в доли секунды. Их называют клеями-расплавами, ибо они не содержат, как правило, растворителей. На их основе делают также липкие ленты, о которых «Химия и жизнь» уже рассказывала (1973, № 8)
Для клеев расплавов не нашлось пока лучшего липкого компонента, чем канифольная смола (или ее производные). И во многих странах канифоль вдруг стала крайне дефицитным продуктом. К тому же у нее появился еще один потребитель — промышленность синтетического каучука: полимеризация многих каучуков идет в эмульсии, и для синтеза требуются тонны эмульгатора — канифоли.
Все эти обстоятельства привели к тому, что производство столь старого материала, как канифоль, продолжает неуклонно расти. Подтверждение этому читатель найдет в таблице.
Производство канифоли в СССР (тонны)
|
Тип канифоли |
Г оды |
||
|
1972 |
| 1973 |
| 1974 |
|
|
Живичная |
97 880 |
111 180 |
116 478 |
|
Экстракционная |
18 640 |
23 030 |
28 217 |
|
Талловая |
11 4,30 |
17 820 |
18 719 |
|
Всего |
127 950 |
152 030 |
163 414 |
Мировое производство канифоли уже превышает миллион тонн. Больше всего выпускают ее в США — около 400 тысяч тонн (причем на первом месте идет галловая, а живичная — на последнем). В КНР делают только живичную канифоль, в Швеции — только талловую.
А КАК НАСЧЕТ СИНТЕЗА?
Наверное, специалистов по канифоли должно бы радовать, что их любимое вещество занимает такие прочные позиции Однако это обстоятельство, как ни странно, радует не слишком: чем больше канифоли, тем больше надо рубить сосны. (Кстати, в этом одна из главных причин, по которой наша страна не увеличивает резко выпуск канифоли.)
Так где же выход? Он, видимо, в синтезе. В конце концов, канифольные смолы — углеводородные, а продукты пиролиза и крекинга нефти именно углеводороды. Правда, намного меньшего молекулярного веса и более просто устроенные, однако из простого можно получить сложное — это ведь и есть синтез.
Из простых углеводородных молекул с помощью катализаторов делают все больше веществ, в том числе и синтетическую канифоль. Правда, настоящую канифоль она напоминает лишь приблизительно — очень уж сложна структура. Вместо абиетиновых и пимаровых кислот получают алифатические смолы, полимеризуя олефины и диолефины (они образуются, в частности, как побочные продукты в производстве изопрена). При этом получаются обычно ненасыщенные смолы, которые слишком легко окисляются на воздухе, но этого можно избежать, если гидрировать смолы (так же, как нередко гидрируют и саму канифоль).
Есть и другие синтетические заменители. Например, полициклические углеводороды, молекулы которых построены из колец неароматической природы. Такие вещества содержатся во многих нефтях, их называют нафтенами; в принципе это простейший заменитель канифоли. Синтетические нафтены бесцветны и прозрачны, они выдерживают действие высоких температур, кислорода и влаги. В Японии их уже выпускают в промышленном масштабе.
Наконец, запатентованы (хотя, насколько автору известно, еще не производятся) синтетические продукты со структурой абиетиновой кислоты Они даже пахнут, как канифоль.
Ну так как же — будущее за синтетической канифолью? Вероятно, да. Говорят, что сравнение — не доказательство, и все же давайте вспомним прошлое, скажем, как после синтеза ализарина стали исчезать плантации марены, как канул в небытие галалит — пластмасса из казеина.
Впрочем, изучая судьбу канифоли, надо обратить внимание на особое обстоятельство: она очень дешева Поэтому вряд ли она уступит свои позиции так же легко, как марена. Ведь рубка лесов будет продолжаться (надеемся, в разумных пределах), и из древесины надо извлечь все полезные вещества, в том числе и канифоль.
И совсем особо надо сказать о талловой канифоли: она будет жить до тех пор, пока бумагу делают не синтетическим путем, а из древесины. Ведь это побочный продукт производства бумаги, и его надо использовать, коль скоро мы стремимся к безотходной технологии. Весьма важно, что талловую канифоль никуда не надо возить — она расходуется там же, где получается, — для проклейки бумаги, А кроме того, талловое масло содержит немало других полезных веществ, например олеиновую и линолевую кислоты, которым тоже есть немало применений.
А. Л. КОЗЛОВСКИЙ